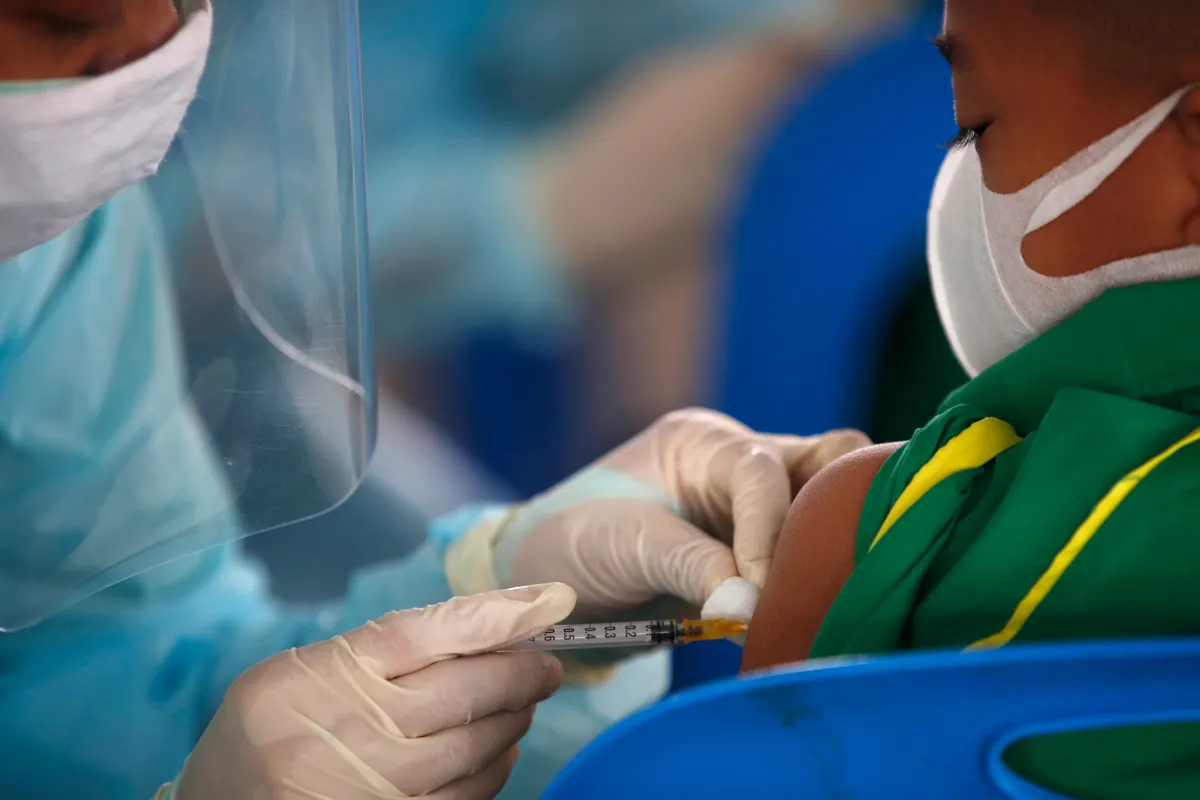
Pfizer y su socio alemán, BioNTech, declararon que un primer análisis demostró que su régimen de tres dosis de su vacuna pediátrica contra el COVID-19 desencadenó una fuerte respuesta inmunitaria en los niños más pequeños, demostrando un 80% de eficacia en la prevención de infecciones sintomáticas en niños de 6 meses a 4 años.
Vacuna COVID-19 de Pfizer
Los resultados, junto con otros avances recientes, indican que la espera de una vacuna para los niños más pequeños, el último grupo que carece de acceso, podría terminar en unas semanas.
- La Administración de Alimentos y Medicamentos (FDA) dijo que los expertos externos de la agencia tienen previsto reunirse el 15 de junio para analizar la vacuna COVID-19 DE Pfizer y otra inyección para los niños más pequeños de Moderna.
- Si el panel asesor de la FDA ve con buenos ojos las vacunas pediátricas, la agencia podría autorizar las inyecciones tan pronto como el 16 o el 17 de junio.
- Los asesores en materia de vacunas de los Centros para el Control y la Prevención de Enfermedades (CDC) estudiarían entonces quiénes deberían recibir las vacunas, y poco después la directora de la agencia, Rochelle Walensky, haría una recomendación final.
- Las vacunas estarían disponibles casi inmediatamente.
- Pfizer dijo que planea terminar de presentar los datos, que no han sido revisados por pares, a la FDA esta semana. Las compañías advirtieron que la cifra de eficacia era fluida porque los resultados aún están llegando.
La vacuna COVID-19 de Moderna para niños
La FDA ya está revisando la vacuna pediátrica de Moderna, un régimen de dos inyecciones que tuvo una eficacia del 51% en la prevención de la enfermedad en niños de entre 6 meses y 2 años, y del 37% en niños de 2 a 5 años.
- Los reguladores habían reservado previamente tres posibles fechas para que los expertos externos de la FDA debatieran sobre las vacunas pediátricas. La más temprana, el 8 de junio, era presumiblemente para Moderna, cuya revisión está más avanzada. Esas reuniones se han cancelado.
- Ahora, el 15 de junio establece una comparación directa de la eficacia y la seguridad del régimen de dos inyecciones de Moderna y la vacuna de tres inyecciones de Pfizer-BioNTech para los niños más pequeños
- Algunos padres reaccionaron con enfado, diciendo que la FDA debería seguir adelante con la reunión del 8 de junio para considerar la vacuna Moderna.
- Según el calendario revisado, la FDA y sus expertos externos debatirán el 14 de junio la vacuna Moderna para niños y adolescentes de 6 a 17 años; la vacuna de Pfizer-BioNTech ya está autorizada para ese grupo de edad.
- Al día siguiente, revisarán las vacunas para los niños más pequeños, con asesores que evaluarán la vacuna Moderna para niños de 6 meses a 5 años y la vacuna Pfizer-BioNTech para niños de 6 meses a 4 años.
- Un documento de planificación de los CDC señala que se espera que las vacunas se envíen inmediatamente después de ser autorizadas por la FDA.
- Los pedidos anticipados de dosis podrían comenzar a finales de mayo o principios de junio, pero la fecha exacta dependerá de cuándo se reúnan los asesores externos de la FDA.
Fuente principal de la noticia: The Washington Post